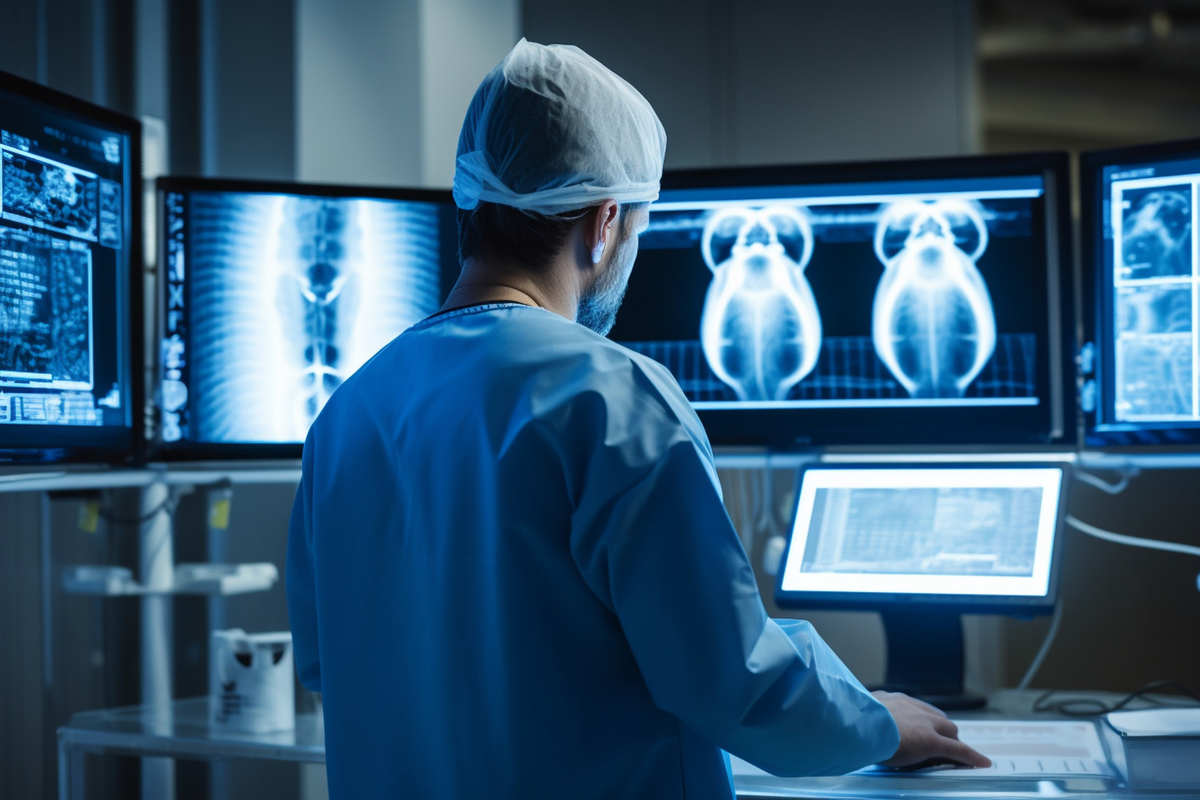
Mythos Nr. 1: Alle digitalen Therapeutika (DTx) sind ziemlich gleich
Mit der Entwicklung der DTx wird die Trennlinie zu den zahlreichen Wellness-Anwendungen auf dem Markt immer deutlicher. Die Unterscheidung besteht im Wesentlichen darin, dass es für DTx klinische Evidenz gibt. Es wäre jedoch zu einfach zu glauben, dass digitale Therapeutika homogen sind. Tatsächlich polarisiert sich der DTx-Markt zunehmend zwischen Lösungen, die auf die Optimierung des Patientenmanagements abzielen, manchmal auch als Digital Care bezeichnet, und solchen, die greifbare physiologische und/oder klinische Effekte erzielen und somit als reine DTx bezeichnet werden können. Jede dieser Gruppen hat ihre Besonderheiten und Möglichkeiten.
Auf der einen Seite dieses Spektrums stehen zahlreiche Lösungen zur Prävention und Behandlung chronischer Krankheiten wie Diabetes und Herz-Kreislauf-Erkrankungen, die eine Verbesserung der Lebensqualität oder eine Senkung der damit verbundenen Gesundheitskosten nachweisen sollen.
Die klinische Validierung dieser Art von DTx kann als relativ einfach angesehen werden (vor allem im Vergleich zur Validierung von Arzneimitteln) und basiert in der Regel auf einem oder zwei einfachen Endpunkten. Omada Health, ein in den USA ansässiger Entwickler von Programmen zur digitalen Lebensstilintervention für die Prävention und Behandlung chronischer Krankheiten, weist beispielsweise auf von Experten begutachtete Studien hin, die zeigen, wie sein digitales Verhaltensberatungsprogramm zur Gewichtsabnahme das Risiko von Diabetes, Schlaganfall und Herzerkrankungen senkt.
Häufig geht es den Entwicklern solcher Lösungen um die Kostenerstattung durch private Krankenversicherungen. So hat Livongo, ein weiterer US-amerikanischer Entwickler einer digitalen Plattform für Patienten mit chronischen Erkrankungen, Partnerschaften mit vier großen nationalen Krankenversicherungen und innovativen Gesundheitssystemen.
Es ist wichtig zu erwähnen, dass die scheinbare Einfachheit dieses Marktes sich allmählich in einen roten Ozean mit hartem Wettbewerb und sehr hohen Kundenakquisitionskosten verwandelt, die manchmal mehrere hundert Dollar betragen.
Auf der anderen Seite werden reine DTx in klinischen Studien getestet, um die klinische Relevanz nachzuweisen, die für die Zulassung durch Gesundheitsbehörden und Kostenerstattung erforderlich ist.
Diese klinischen Studien ähneln im Allgemeinen eher den traditionellen Arzneimittelstudien und zielen auf sehr spezifische Endpunkte ab. So finanziert Oncomfort, ein belgischer Entwickler einer auf virtueller Realität basierenden Hypnoselösung zur Linderung von Schmerzen und Ängsten, eine klinische Studie, in der die Wirkung von Schmerzreizen mit und ohne seine Lösung verglichen wird, indem physiologische und neurophysiologische Veränderungen beobachtet werden, die von Sensoren und Captoren aufgezeichnet werden. Ein weiteres erfolgreiches Beispiel aus jüngster Zeit ist Somryst, ein verschreibungspflichtiges digitales Therapeutikum für Patienten mit chronischer Schlaflosigkeit, das von Pear Therapeutics entwickelt und von der FDA im Rahmen eines herkömmlichen Verfahrens für Medizinprodukte im Jahr 2020 zugelassen wurde. Es wurde klinisch nachgewiesen, dass mit Somryst verbundene neuropsychologisch Interventionen zu einer Verbesserung des Schweregrads der Schlaflosigkeit sowie der Einschlaflatenz und des Aufwachens nach dem Einschlafen führen.
Der Nachteil des Ziels, einen soliden Nachweis des klinischen Nutzens und der Kostenerstattung zu erbringen, besteht darin, dass die DTx-Akteure zum Beispiel langwierige Verfahren durchlaufen müssen, sich an hochrangigen wissenschaftlichen und medizinischen Diskussionen über die Auswahl der Endpunkte beteiligen müssen oder mit Regulierungsbehörden und Kostenträgern verhandeln müssen.
Erfahren Sie mehr über das Potenzial und die Entwicklung von DTx im Gesundheitswesen >
Mythos Nr. 2: Alle DTx sind Einzellösungen, die mit Medikamenten konkurrieren
DTx scheinen eine Alternative zu traditionellen pharmakologischen Lösungen zu sein. Mit Ausnahme seltener Beispiele wie Oncomfort sind digitale Therapien jedoch nicht als Ersatz für pharmakologische Behandlungen gedacht, sondern eher als Vorstufe (z.B., zur Krankheitsprävention) oder als Ergänzung und Verbesserung. So zielen verschiedene DTx-Lösungen darauf ab, die Therapietreue der Patienten durch digitale Interventionen zu verbessern. DTx, die auf die Verbesserung spezifischer patientenrelevanter Endpunkte abzielen, werden häufig auch in Kombination mit Medikamenten eingesetzt. Akili, ein weiteres US-amerikanisches Unternehmen für verschreibungspflichtige digitale Medizin, sponsert beispielsweise eine klinische Studie, die die Wirkung seiner Software in Kombination mit stimulierenden Medikamenten bei Patienten mit Aufmerksamkeitsdefizit-Hyperaktivitätsstörung (ADHS) nachweisen soll.
Vor diesem Hintergrund besteht eines der Dilemmas des Geschäftsmodells von DTx darin, zu entscheiden, ob es mit spezifischen Medikamenten gebündelt werden soll, um eine umfassende patientenorientierte Lösung anzubieten, oder ob es als eigenständiges Produkt vermarktet werden soll, das in der Lage ist, die Ergebnisse der Patienten in Kombination mit verschiedenen pharmakologischen Behandlungen zu verbessern.
Mythos Nr. 3: DTx sind eine Spielwiese für reine Technologieunternehmen
In der Tat erfordert die Entwicklung von DTx herausragende digitale Kompetenzen und die Agilität, iterativ benutzerfreundliche Lösungen zu entwickeln – Eigenschaften, die eher bei digitalen Start-ups als bei traditionellen Pharmaunternehmen zu finden sind. Auf DTx spezialisierte Unternehmen arbeiten jedoch häufig mit Pharmaunternehmen zusammen, um von deren Forschungsexpertise, umfassender Erfahrung mit behördlichen Zulassungs- und Erstattungsverfahren sowie Verständnis für Kostenträger und klinische Praktiken zu profitieren.
Die Vorteile einer solchen Symbiose sollten regelmäßig neu bewertet werden, um zu entscheiden, ob die Zusammenarbeit fortgesetzt werden soll, wie die bereits erwähnte Partnerschaft zwischen Novartis und Pear Therapeutics, einem Entwickler verschreibungspflichtiger DTx, zeigt. Seit 2018 entwickeln die beiden Unternehmen gemeinsam DTx-Lösungen zur Behandlung von Schizophrenie und Multipler Sklerose. Während diese Zusammenarbeit offenbar fortgesetzt wird, hat sich Sandoz (ein Unternehmen von Novartis) Ende 2019 aus der geplanten gemeinsamen Vermarktung von reSET, einem verschreibungspflichtigen DTx zur Behandlung von Drogenkonsumstörungen, zurückgezogen.
DTx-Entwickler und Pharmaunternehmen profitieren nicht nur von einer Reihe sich ergänzender Kompetenzen, sondern können auch Synergien erzielen, indem sie einen stärker vernetzten Raum für Patientendaten schaffen. Ein gutes Beispiel ist die Partnerschaft zwischen Roche und mySugr, einer der weltweit beliebtesten digitalen Diabetes-Plattformen. Das vernetzte Blutzuckermessgerät Accu-Chek von Roche wird von der FDA-zugelassenen Diabetes-Management-App Accu-Check Connect begleitet, mit der Patienten ihren Blutzuckerspiegel überwachen können und die mit der umfassenden Diabetes-Management-Plattform mySugr synchronisiert ist.
Zusammenfassend lässt sich sagen, dass sich für Pharmaunternehmen nicht mehr die Frage stellt, „ob sie sich auf digitale Therapeutika einlassen sollen oder nicht“, sondern „wie sie in einem Umfeld erfolgreich sein können, in dem DTx zu einem integralen Bestandteil von Behandlungsschemata werden“. In diesem Zusammenhang müssen Pharmaunternehmen das relevanteste Nutzenversprechen für die zu entwickelnden DTx entschlüsseln, entscheiden, wie diese in das bestehende Medikamentenportfolio integriert werden können (in Kombination oder allein) und den richtigen Partner für das weitere Vorgehen auswählen.
Über die Autoren,
Benjamin, Great Explorer Digital Health in Alcimeds Healthcare Team in Frankreich
Luc, Partner und Business Unit Director in Alcimeds Healthcare Team in Frankreich
Amélie, Head of Data in Alcimeds Healthcare Team in Frankreich